对乳腺癌患者而言,手术切除病灶只是康复第一步。术后残留的微小病灶如同“定时炸弹”可能导致复发,而乳腺组织缺损与泌乳功能丧失更造成身心双重创伤。
近日,先进药物递释系统全国重点实验室、浙江大学药学院、金华研究院顾臻教授、俞计成教授团队,联合苏州大学王慎强教授团队和山东大学胡慧丽教授团队,在Nature Biomedical Engineering上发表了题为:“Mammary organoid-based depot for post-surgical chemotherapy and gland regeneration”的研究,另辟蹊径将乳腺类器官改造为一座模拟“泌乳”的活体药物工厂——既能持续释放化疗药物清扫残余肿瘤,又能像“活的种子”融入宿主,引导功能性乳腺腺体重建(图1)。
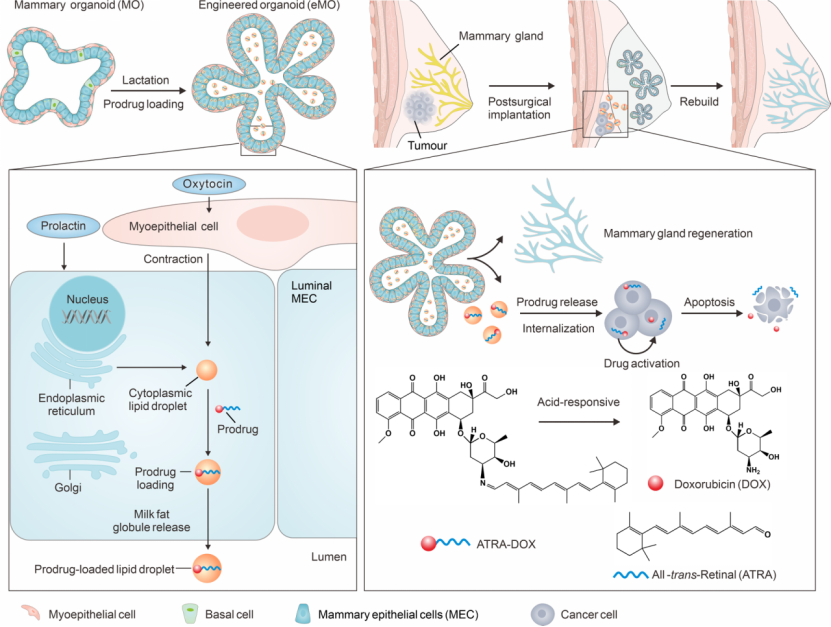
图1. 工程化乳腺类器官的构建及肿瘤术后化疗与乳腺再生示意图
类器官是利用干细胞体外三维培养而成的微型器官模型。乳腺类器官拥有外层的肌上皮细胞与内层的管腔上皮细胞,具备与真实乳腺相似的收缩与分泌潜能。研究团队首先通过体外诱导使其进入类似“泌乳”的成熟状态,此时内部管腔细胞会自发合成并储存大量富含脂质的微小油滴(脂滴)(图2a)。团队合成了一种由全反式视黄醛(ATRA)与阿霉素(DOX)通过酸敏化学键连接的前药分子。因其出色的亲脂性,该前药能高效“躲进”类器官脂滴内,载药效率高达85.3%,远超未经诱导的普通类器官,且对类器官自身几乎无毒(图2b)。
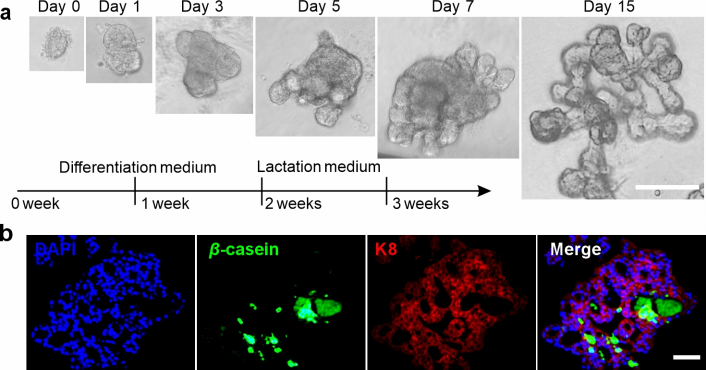
图2. 工程化乳腺类器官药物储库的构建。a,乳腺类器官培养过程中不同时间点显微镜照片,比例尺:200 μm。b,工程化乳腺类器官免疫荧光染色图,绿色:乳汁蛋白,红色:腔管细胞,比例尺:50 μm。
当装载前药的工程化类器官植入小鼠乳腺癌术后残腔,在体外催乳素等信号作用下,外层肌上皮细胞开始节律性自主收缩,将负载前药的脂滴持续释放至周围。载药脂滴抵达残余肿瘤特有的弱酸性微环境后,酸敏化学键断裂,阿霉素与ATRA联手精准打击残留肿瘤细胞:阿霉素杀伤增殖细胞,ATRA削弱肿瘤“干性”克服耐药。体内实验显示,该策略使小鼠乳腺癌术后复发率降至25%,75%受治小鼠生存超100天,疗效远超对照组。免疫分析表明,持续释放的药物与脂滴共同激活机体抗肿瘤免疫,瘤内杀伤性T细胞增多、抑制性调节T细胞减少,“冷”肿瘤微环境被成功逆转。
与传统的合成支架或惰性填充物不同,类器官能够主动与受体小鼠的乳腺脂肪垫组织发生整合。在完成药物分泌使命后,这些类器官并未消失,而是作为“种子”细胞,在宿主体内逐渐分化、延伸,形成新的乳腺导管分支结构。当受治母鼠受孕后,再生的乳腺组织成功响应了生理信号,恢复了分泌乳汁的功能。
为使这一策略更贴近临床现实,研究团队进一步利用人诱导多能干细胞(iPS细胞),通过精细的时序调控与因子诱导,成功在体外培育出具备完整结构的人源化乳腺类器官。在构建的人源化乳腺癌异种移植模型中,工程化人源类器官同样显著抑制了术后肿瘤复发,并推动了人源化乳腺导管在免疫缺陷小鼠体内的生长与整合。
该研究展示了全新的仿生递药理念:利用人体自身生理机制,将微型器官转化为智能、长效且兼具再生功能的治疗平台。团队正将该技术拓展至其他实体瘤术后治疗与相应器官修复。未来结合患者自体干细胞培育个性化类器官,有望真正实现个性化的精准治疗与自体重建一体化。
原文链接:https://www.nature.com/articles/s41551-026-01655-1








